热解(Pyrolysis)、热催化(Thermocatalysis)、气化(Gasification)是三种常见的高温化学处理过程,它们在化学反应、产物组成、应用等方面有明显的区别。以下是它们的主要区别:
1. 热解(Pyrolysis)
定义:
热解是指在高温下,在缺氧或无氧环境中,通过热能使有机物(如煤、木材、塑料等)发生分解反应。热解过程没有氧气的参与,因此有机物不会完全燃烧,而是转化为气体、液体和固体产物。
反应机理:
- 热解通常发生在500°C到900°C之间的高温环境中。在此温度下,大分子有机物在热能的作用下分解为小分子。
- 反应是物理和化学的共同作用,高温下的化学键断裂是分解的主要驱动力。
- 热解过程没有氧气或氧气极少,避免了氧化反应,产生的是碳氢化合物的裂解产物。
产物:
- 气体:包括甲烷(CH₄)、乙烯(C₂H₄)、丙烯(C₃H₆)、氢气(H₂)、一氧化碳(CO)等。
- 液体:主要是轻油(或称为焦油),其中包含许多有机化合物,包括烃类和其他有机化合物。
- 固体:焦炭、炭黑或其他固体碳残渣。
应用:
- 废弃物处理:热解用于废塑料、橡胶、木材和农业废弃物的处理,能够回收资源并减少环境污染。
- 生物质转化:在生物质(如木屑、稻草等)的能源转化中,热解提供了一个重要的替代能源路径。
- 炭黑生产:通过热解过程可以生产炭黑,这是一种广泛用于轮胎制造和其他工业用途的原材料。
优缺点:
- 优点:不需要氧气,适合氧敏感物质;能获得多种产品(气、油、炭)。
- 缺点:能量消耗较高,产物中焦油较难进一步利用;过程需要高温设备。
2. 热催化(Thermocatalysis)
定义:
热催化是指在高温条件下,利用催化剂加速某些化学反应的过程。催化剂在反应过程中并不被消耗,它通过降低反应的活化能来加速反应的速率,从而在较低的温度下实现目标产物的转化。
反应机理:
- 热催化过程的本质是利用催化剂来促进反应,催化剂通常是金属、金属氧化物或其他化学物质。
- 在热催化过程中,催化剂通过提供一个低能量的反应途径来加速反应。例如,催化裂化中,催化剂可以帮助烃类分子断裂生成小分子烃(如丙烯、乙烯等)。
- 高温下的催化反应通常与传统的热解有所不同,因为催化剂控制了反应的方向和速率。
产物:
- 轻烃:如乙烯(C₂H₄)、丙烯(C₃H₆)、丁烯等,用于石化行业。
- 油品:加氢裂化和催化裂化等过程产生的燃料油或柴油。
- 氢气:在加氢反应中生成氢气,常用于石油精炼。
- 其他:气体、芳香烃、脂肪烃等。
应用:
- 石油化工:催化裂化、加氢裂化、加氢脱硫等过程广泛应用于石油加工,用于生产汽油、柴油和其他化学品。
- 合成气生产:催化加氢合成气(氢气+一氧化碳)用于进一步制备甲醇、氨等化学品。
- 废气处理:热催化反应在汽车尾气和工业废气的处理上也有应用,催化剂可以帮助去除有害气体。
优缺点:
- 优点:通过催化剂提高反应效率,能够选择性地产生所需产物,减少副产物。
- 缺点:催化剂的选择和寿命是关键,需要定期更换;部分反应可能产生不期望的副产物。
3. 气化(Gasification)
定义:
气化是指将固体燃料(如煤、生物质或废物)在高温和有限氧气或水蒸气的条件下,转化为可燃气体(合成气)的过程。气化不仅仅是简单的燃烧,而是一个氧化还原反应,目的是产生富含氢气、一氧化碳、甲烷等的气体。
反应机理:
- 气化过程通常发生在800°C到1200°C之间,反应中需要有限量的氧气或水蒸气。气化反应的基本原理是:固体燃料与氧气或水蒸气反应生成气体产物。
- 气化的反应可以分为两个阶段:
- 干馏阶段:固体物质在热解过程中被分解成挥发性物质,释放出一部分气体。
- 气化阶段:剩余的固体和氧气/水蒸气反应,生成一氧化碳、氢气和甲烷等气体。
产物:
- 合成气:主要由一氧化碳(CO)、氢气(H₂)、甲烷(CH₄)、二氧化碳(CO₂)等组成。
- 焦炭:部分固体残渣未完全气化,形成焦炭。
- 少量液体:气化过程中也可能生成液体,如焦油。
应用:
- 合成气生产:合成气(CO + H₂)是许多化学反应的原料,常用于生产甲醇、氨、合成燃料等。
- 清洁能源:气化过程可以将低质量的煤或生物质转化为清洁的合成气,是一种比较环保的能源转化方法。
- 废弃物处理:废弃物气化不仅可以减少固体废物的体积,还能回收能量(如产生电力或热能)。
优缺点:
- 优点:能够高效地从煤、生物质、废物等转化为可用的合成气,气化过程比传统燃烧更为环保。
- 缺点:需要较高的温度和压力,设备复杂;气化产物的控制较为困难,可能会产生不稳定成分。
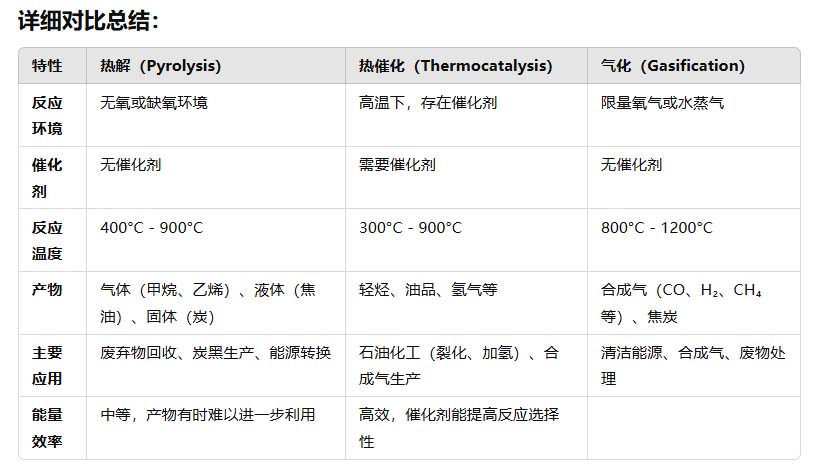
总结:
- 热解侧重于在无氧环境下分解有机物,通常产生气体、油和炭。
- 热催化是利用催化剂促进高温下的化学反应,产生目标产物,如轻烃或油。
- 气化通过在氧气或水蒸气的参与下,将固体燃料转化为合成气,用于能源生产或化学合成。















